V oblasti topenářství dochází ke korozní degradaci kovových konstrukčních materiálů převážně ve vodném prostředí a koroze zde má velmi často elektrochemický charakter. Elektrochemická reakce je spojená s přenosem náboje a účastní se jí tedy látky, které přijímají nebo ztrácejí elektrony a mění se jejich oxidační stupeň. Korozní elektrodové reakce jsou tedy oxidačně – redukční, a proto zde probíhají dvě dílčí reakce – anodická a katodická. Anodické reakci odpovídá oxidace kovu – vlastní koroze. Katodická část zahrnuje redukci některé oxidované složky obsažené v roztoku a nazývá se reakcí depolarizační.
Povrch kovu je rozdělen na anodická a katodická místa, na nichž probíhá odděleně korozní, resp. depolarizační reakce. V nejjednodušším případě, kdy kov koroduje na celém svém povrchu rovnoměrně, mají anody a katody velikost atomu a jejich poloha se neustále mění. V případech tzv. nerovnoměrných forem koroze probíhají jednotlivé reakce přednostně na určitých částech povrchu kovového materiálu. Nejčastěji to bývá způsobeno usnadněným přístupem některé aktivní složky prostředí k jedné části povrchu.
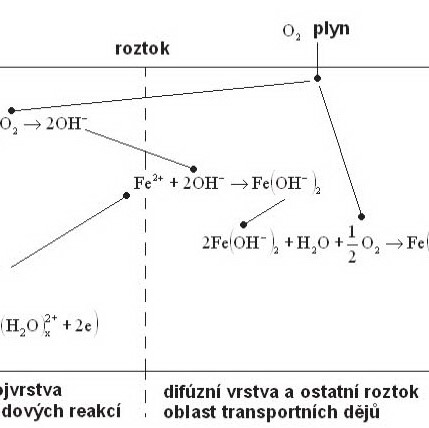
Schematické znázornění dějů při korozi železa

Schéma znázorňuje průběh základních dějů probíhajících při korozi železa v neurálním prostředí. Je zde znázorněna elektrická dvojvrstva u povrchu kovu, ve které probíhají dílčí elektrodové reakce (anodická a katodická) a difúzní vrstva, která je významná zejména z hlediska přísunu reagujících látek z roztoku a odvodu reakčních produktu od povrchu kovu, zajišťující tak trvalý korozní průběh. Důležité jsou i následné reakce primárních produktů mezi sebou nebo s látkami obsaženými v roztoku, které mohou vést k vzniku tuhých korozních zplodin.